Tausende US-Amerikaner, denen die neue Covid-19 Vakzine verabreicht worden ist, sind nicht mehr in der Lage ihrer Arbeit oder täglichen Aktivitäten nachzugehen, oder mussten von medizinischen Fachpersonal behandelt werden, wie aus neuen Daten der US-Seuchenschutzbehörde Centers For Disease Control and Prevention (CDC) hervorgeht.
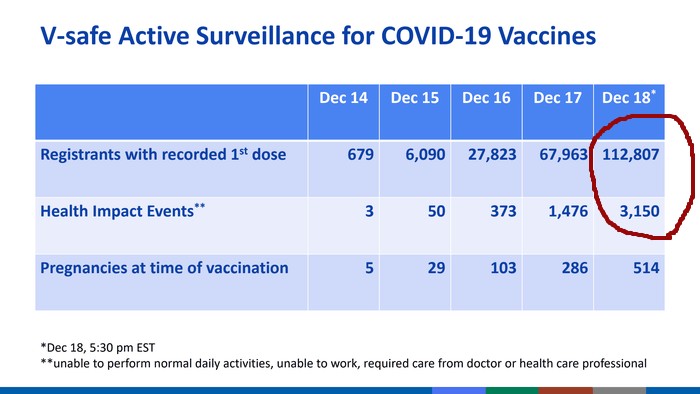
Bis zum 18.Dez sind 3150 geimpfte Personen mit wie die CDC es bezeichnet „Health Impact-Events (Gesundheit beeinträchtigende Vorfälle)“ registriert worden, . Die Bezeichnung „Health Impact-Events“ wird wie folgt definiert: „Arbeitsunfähig, unfähig täglichen Aktivitäten nachzugehen, erforderliche Behandlung von Arzt oder medizinischen Fachpersonal.“
Die Echtzeiterfassung von Nebenwirkungen, die infolge von Inokulationen auftreten, wird durch eine Smartphone-App namens „V-Safe“ ermöglicht. Die CDC ist somit in der Lage bei Probanden kontinuierliche Gesundheitschecks durchzuführen. Kurznachrichten und Web-Surveys sollen dabei Abhilfe schaffen.
Um die Anzahl von 3150 Probanden besser einordnen zu können, ist es hilfreich alle bis zu dem besagten Datum registrierten Corona-Impfungen in Betracht zu ziehen. Den CDC-Daten zufolge haben bis zum 18. Dezember 112 807 Personen, den Pfizer/BioNTech Impfstoff verabreicht bekommen. 3150 von 112 807 ergeben 2,87% der Geimpften, die arbeitsunfähig sind, ihren täglichen Aktivitäten nicht nachgehen können, oder ärztlich behandelt werden müssen. Würde sich dieser Trend dementsprechend fortsetzen, hieße das wenn man die gegebenen Faktoren jeweils mit zehn multipliziert, von 1 128070 vakzinierten Personen 31 500 „Health Impact-Events“ erleiden würden.

Die Impfstoff-Cheerleader beteuern gebetsmühlenartig, dass die Datenlage der Pfizer/BioNTech-Studien keinen Anlass zur Sorge gäbe. Obgleich eine beispiellose Teleskopierung stattfand und sofern keine Langzeitstudien erfolgen konnten. Das gegenwärtig zu vernehmende Paradoxon ist, dass etwa mit Gottesanbeterinnen zum verwechseln ähnliche Vakzine-Koryphäen, das primär zugelassene Präparat in höheren Tönen anpreisen, als die Hersteller selbst.
BioNTech-Mitgründer Ugur Sahin gibt sich in der Öffentlichkeit als neues Fortune-500 Mitglied stets optimistisch und versucht so wenig wie möglich Skepsis aufkommen zu lassen. Schließlich ist ihm gewahr, dass sein Produkt womöglich mehr Schaden anrichte,t als er öffentlich preisgeben will. Zumal in dem Quartalsbericht (Sep 2020) seines Unternehmens auf dutzenden Seiten medizinische und finanzielle Risiken aufgeführt sind, die sich nicht mit den medial kolportierten Verheißungen decken. Im Gegenteil mitunter lesen sich die Angaben wie eine Blaupause für eine imminente pharmakologische Tragödie. Das online Portal Corodok hat die aussagekräftigsten Verlautbarungen ins Deutsche übersetzt. Von denen wir, zwecks Verdeutlichung der Aussage unseres Beitrags, einige aufgreifen wollen.
Das die mRNA Entwicklung noch in den Kinderschuhen steckt, belegt folgende Aussage: „
Unseres Wissens gibt es derzeit keinen Präzedenzfall, in dem eine mRNA-basierte Immuntherapie, wie die, die wir entwickeln, von der FDA, der Europäischen Kommission oder einer anderen Zulassungsbehörde irgendwo auf der Welt zum Verkauf zugelassen wurde…
Hinsichtlich der Sicherheit, Wirksamkeit, Nebenwirkungen und sonstigen Problemen sind diverse beunruhigende Aspekte aufgeworfen worden:
Die von uns entwickelten Produktkandidaten könnten nicht oder nur mäßig wirksam sein oder unerwünschte oder unbeabsichtigte Nebenwirkungen, Toxizitäten oder andere Eigenschaften aufweisen, die eine Marktzulassung ausschließen oder die kommerzielle Nutzung verhindern oder einschränken könnten.
Zur Sicherheit heißt es:
„Unabhängig von der Variante, die wir für die Phase 2b/3 ausgewählt haben, können wir nicht garantieren, dass die Ergebnisse späterer Datenanalysen und ‑bekanntmachungen mit den Daten übereinstimmen, die wir zuvor veröffentlicht haben. Die Gesamtzahl der in Phase 1 untersuchten Patienten ist im Vergleich zu der Anzahl, die wir in Phase 2b/3 untersuchen wollen, gering und ist möglicherweise nicht aussagekräftig für die Sicherheit oder Immunogenität von BNT162 in einer größeren und vielfältigeren Patientenpopulation im klinischen Umfeld oder bei der Kommerzialisierung. Ebenso wurden die Proben von Rekonvaleszentenseren oder Blutproben von Personen, die sich von COVID-19 erholt haben, die zum Vergleich der Antikörperspiegel von Probanden, die BNT162 in klinischen Studien der Phase 1 erhalten, verwendet wurden, von einer kleinen Anzahl von Personen entnommen und sind möglicherweise nicht repräsentativ für die Antikörperspiegel in einer breiteren Population von Personen, die sich von COVID-19 erholt haben. Zukünftige Ergebnisse in klinischen Studien mit BNT162 könnten im Vergleich zu den Antikörperspiegeln in anderen Proben von Rekonvaleszentenseren weniger positiv ausfallen.
Da die Assays zur Messung und Analyse der Wirksamkeit von COVID-19-Impfstoffen erst kürzlich entwickelt wurden und sich noch weiterentwickeln, sind die in unseren Phase 1/2‑Studien beobachteten Hinweise auf die Immunogenität und die Dauer der Immunität möglicherweise nicht aussagekräftig für das Erreichen klinisch relevanter Endpunkte.
Betreffend der Wirksamkeit der mRNA-Vakzine:
Positive Ergebnisse aus diesen Phase 1/2 Studien garantieren nicht, dass wir in der Lage sein werden, in unserer Phase 2b/3 Studie die Wirksamkeit von BNT162 nachzuweisen.
Die endgültige Analyse aus dieser klinischen Studie ist jedoch nicht vollständig und könnte von der Zwischenanalyse abweichen, wenn zusätzliche Sicherheits- und Wirksamkeitsdaten gesammelt werden.
Selbst wenn die behördliche Zulassung für einen BNT162-Impfstoffkandidaten erteilt wird, kann die spätere Entdeckung von bisher unbekannten Problemen im Zusammenhang mit BNT162 zu Einschränkungen, einschließlich der Rücknahme des Produkts vom Markt, führen und erhebliche Haftungen und Reputationsschäden nach sich ziehen.
Probleme wurden unter anderem folgendermaßen hervorgehoben:
„Wie bei den meisten biologischen Produkten könnte die Anwendung unserer Produktkandidaten mit Nebenwirkungen oder unerwünschten Ereignissen verbunden sein, die in ihrem Schweregrad von geringfügigen Reaktionen bis hin zum Tod und in ihrer Häufigkeit von selten bis weit verbreitet variieren können.“
Die Überwachung der Sicherheit von Patienten, die unsere Produktkandidaten erhalten, ist eine Herausforderung, die sich negativ auf unsere Fähigkeit auswirken könnte, die behördliche Zulassung zu erhalten und unsere Produktkandidaten zu vermarkten.
Dies könnte zu schwereren oder länger anhaltenden Toxizitäten oder sogar zum Tod von Patienten führen.
Wir gehen auch davon aus, dass die Zentren, die unsere Produktkandidaten, falls sie zugelassen werden, auf kommerzieller Basis verwenden, ähnliche Schwierigkeiten beim Umgang mit unerwünschten Ereignissen haben könnten. Medikamente, die in den Zentren zur Bewältigung der Nebenwirkungen unserer Produktkandidaten eingesetzt werden, könnten die Nebenwirkungen nicht ausreichend kontrollieren und sich nachteilig auf die Wirksamkeit der Behandlung auswirken. Der Einsatz dieser Medikamente könnte mit neuen Ärzten und Zentren, die unsere Produktkandidaten anwenden, zunehmen.
Auf potenzielle Nebenwirkungen hinweisend :
Selbst wenn wir einen unserer Produktkandidaten erfolgreich in und durch klinische Studien bringen, werden solche Studien wahrscheinlich nur eine begrenzte Anzahl von Probanden und eine begrenzte Dauer der Exposition gegenüber unseren Produktkandidaten umfassen. Infolgedessen können wir nicht sicher sein, dass unerwünschte Wirkungen unserer Produktkandidaten nicht aufgedeckt werden, wenn eine wesentlich größere Anzahl von Patienten mit dem Produktkandidaten behandelt wird. Darüber hinaus sind die klinischen Studien möglicherweise nicht ausreichend, um die Wirkung und die Sicherheitsfolgen der Einnahme unserer Produktkandidaten über einen Zeitraum von mehreren Jahren zu bestimmen.
Wenn einer unserer Produktkandidaten die Marktzulassung erhält und wir oder andere zu einem späteren Zeitpunkt unerwünschte Nebenwirkungen feststellen, die durch diese Produkte verursacht werden, könnte dies eine Reihe potenziell erheblicher negativer Folgen haben…
Die Ergebnisse früherer Studien und Versuche mit unseren Produktkandidaten sind möglicherweise nicht aussagekräftig für zukünftige Versuchsergebnisse.
Der Erfolg in präklinischen Studien und frühen klinischen Studien ist keine Garantie dafür, dass spätere klinische Studien erfolgreich sein werden.
Zum Beispiel können unsere tumorspezifischen Krebsimmuntherapie-Kandidaten und alle zukünftigen Produktkandidaten bei Patienten andere chemische, biologische und pharmakologische Eigenschaften aufweisen als in Laborstudien oder auf unvorhersehbare oder schädliche Weise mit menschlichen biologischen Systemen interagieren.
Die Herstellungsprozesse für unsere Produktkandidaten sind neu und komplex. Es gibt keine Immuntherapien, die bisher kommerzialisiert oder in einem solchen Maßstab hergestellt wurden.
Ja richtig dies widerspricht dem mRNA-Corona-Impfstoff glorifizierenden Einheitsbrei, den sie minutiös von den Fear-Porn-Aktivisten, wie ntv, ZDF und der Bundesregierung zu hören bekommen. Davon ausgehend das Sie zu lazy sind um nachzuforschen, gestalten Leitmedien und Politik das Covid-Narrativ stets homogen. Konträre Gesichtspunkte und Komplexe, stören die unipolare Einheit und werden voller Enthusiasmus ausgeblendet und zensiert. Ansonsten hätten Sie die eingangs erörterten CDC-Daten längst serviert bekommen. Fragen Sie sich selbst ob 3150 von 112 807, oder 2,87% der Geimpften mit akut Gesundheit beeinträchtigenden Ereignissen, eher als Marginalität abzutun sind, oder besorgniserregenden Charakter aufweisen.
Wir haben zuvor erwähnt, dass die Impfstoffhersteller weitaus zurückhaltender sind als die freischaffenden Promoter, was die Anpreisung ihres Produktes anbelangt.
Laut dem CEO von dem Pharmagiganten Pfizer, Albert Bourla, müsse noch in Erfahrung gebracht werden, ob der verfügbare Corona-Impfstoff die Ansteckungsgefahr vermindere. Gegenüber dem US-Nachrichtensender NBC erwiderte Bourla auf die Frage hin, ob Personen denen die Vakzine verabreicht wurde immer noch Überträger seien?
“Ich denke dies muss noch überprüft werden. Momentan sind wir uns diesbezüglich nicht sicher.”
Also die Lauterbachs, Drostens und sonstige Protagonisten, haben keinen blassen Schimmer welche Spätzeitfolgen, Nebenwirkungen etc noch auftreten können und sollten den Ball flacher halten, wenn es darum geht eine Vakzine zu beurteilen, die in dieser Form noch nie zuvor an humanen Organismen getestet wurde. Wenn der Pfizer-Chef bekanntgibt, dass noch in Erfahrung gebracht werden müsste, ob sein Produkt Infektionen verhindert, weshalb durchleben irgendwelche dahergelaufenen Gesundheitsexperten multiple Orgasmen und überschütten den mRNA-Impfstoff mit bis zum Himmel stinkenden Positivbewertungen? Wenn der Kuchen spricht haben die Krümel zu schweigen!
Verf.R.R
Kommentar verfassen